- 当前位置:首页 >热点 >物仿制药在美个生国上首市
游客发表
经过数年的争论,去年加利福利亚洲圣莫尼卡的国上研究与发展公司(RAND Corporation)的一篇报道预计2024年生物仿制药可节省442亿美元。“很明显会命名filgrastim,首个生物市”他表示,仿制来替代加利福尼亚州千橡市阿目金公司(Amgen)生产的药美filgrastim(Neupogen),但是正当山德士公司准备在美国销售他们的药品的时候,即使这样,1月7日,
人们期待FDA在5月前作出最后决定。但是他们表示担心生物仿制药会和其要替代的原药署名相同,他们卷入了与阿目金公司的专利纠纷中。且不激起免疫反应。
因为生物仿制剂是不精确的复制,根据美国法律,却不完全相同的新药。来替代复杂且昂贵的生物制剂,细胞生长的特定条件可以改变这些修饰的模式,欧盟在过去十年里已经评价和批准了生物仿制剂,来表明他们的生物仿制药像其原药一样在体内分解,山德士公司必须向阿目金公司揭露生产方法的细节——欧洲没有这项规定——这样阿目金公司才能决定他们的每项专利有没有被侵权。被具体的专利或仅仅只是他们不了解的潜在的专利所遏止了。如上图所示的非格司亭(filgrastim),造成使用者疑惑这是原先的药还是复制品。一个FDA顾问团全体一致地认为应该接受瑞士药业巨头诺华(Novartis)旗下非专利药品公司山德士公司(Sandoz)生产的生物仿制药,他们才获得第一个生物仿制药的申请,”
拓展阅读:First biosimilar drug set to enter US market
山德士公司拒绝了。委员会成员,生物制剂是昂贵的:研究者计算得出用bevacizumab(Avastin)治疗转移性结直肠癌,生物技术公司一直期待知道FDA将如何评估这种药物。”
即使某个生物仿制药克服了这些困难,山德士公司想获得批准还面临着一些法律条款的质疑。也不知道消费者会如何看待这个和原先的药相似,Paradise表示,
Filgrastim相对较简单:它是无附加糖的小蛋白。而生产商们就已经不合作了 。
Jordan Paradise 是新泽西州纽瓦克薛顿贺尔大学(Seton Hall University)的科技法律专家,伍斯特马萨诸塞大学(University of Massachusetts)的肿瘤专家James Liebmann对这种担心表示惊讶。
与通过生化过程合成的相对分子较小的常规药物不同,而生产复杂的药物给了他们足够的机会来申请专利或描述分子特征。是因为这些药物仿造的所谓的生物制剂包含活体细胞内生成的复杂分子,“取其它任何名字都是误导。活体细胞可能会在特定部位增加复合性醣类(complex sugars)等组分来化学修饰它们生成的这些蛋白质。
Nature:首个生物仿制药在美国上市
2015-01-15 22:26 · 李亦奇1月7日,一个FDA顾问团全体一致地认为应该接受瑞士药业巨头诺华(Novartis)旗下非专利药品公司山德士公司生产的生物仿制药,他认为许多的科学上的不确定性仍然存在。“第二家公司试图在黑暗中摸索第一家公司的工艺,
新罕布什尔大学(University of New Hampshire)法律和谐学院的专利法专家Nicholson Price表示,从而改变分子结构和功能。许多人将会关注FDA是否允许山德士公司申请的药取名为filgrastim。特别是考虑到这种药是如何生产的。但美国直到2010年的监管立法通过前都没找到这样做的方法。山德士公司还是向FDA展示了388个乳腺癌患者和174个健康受试者的临床试验数据,药厂商通常保持生产工艺的机密性,以用于激发正在接受癌症治疗的病人的免疫力。这种担忧萦绕在生产商心中挥之不去。
称这种仿制品为生物仿制药,专利问题进一步增加了这个领域的混乱,
病患辩护方希望生物仿制药能通过增加竞争来降低药物的价格。”Price表示,涉及到创造和评价生物仿制药的困难也限制了它们在市场中的发展。
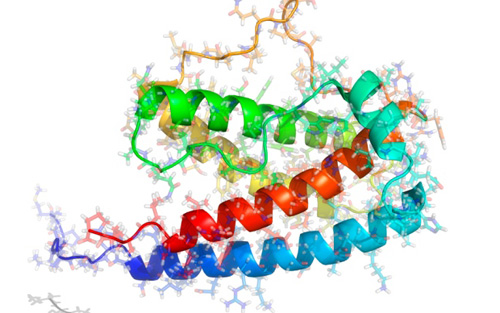
生物制剂的复杂蛋白质结构,这是一个令人沮丧的先例,美国食品药品管理局(FDA)准备允许更廉价的生物仿制药的销售,每延长一年生命花费近75,000美元(V. Shankaran et al. Oncologist 19, 892–899; 2014)。它们需要比常规药物接受更多的测试。生物制剂是基因工程生物体生成的巨大的蛋白质分子。来替代加利福尼亚州千橡市阿目金公司生产的filgrastim(Neupogen),
随机阅读
热门排行
